杭州师范大学附属医院车先伟教授团队在Neurotherapeutics发表了名为 Identifying neural circuitry abnormalities in neuropathic pain with transcranial magnetic stimulation and electroencephalogram co-registration 的文章。
一、研究背景
神经病理性疼痛(NP)是一种典型的难治性慢性疼痛,全球约有10%的人群深受其扰。近年来,非侵入性脑刺激(NIBS)技术在神经病理性疼痛方面展现出了巨大潜力。其中,重复经颅磁刺激(rTMS)和经颅直流电刺激(tDCS)等技术备受关注。然而,关于rTMS镇痛作用在神经病理性疼痛中的神经回路基础,目前仍不明确。为了深入探究这一问题,研究采用了单脉冲经颅磁刺激(TMS)结合脑电图(EEG)评估大脑皮层的不同连接性。通过TMS-EEG,研究者能够对关键通路的电流传播进行表征,包括下行通路、注意力认知疼痛通路以及情感疼痛通路。研究中还引入了两个重要的指标:显著电流密度(SCD)和显著电流传播(SCS)。显著电流密度是对TMS诱发EEG活动的局部源电流密度的度量,而显著电流传播则是从TMS靶点(M1)到特定脑区电流扩散的累积距离。
二、研究方法
1、TMS刺激设置
TMS线圈被放置在与中线成45°角的位置,刺激强度被设置为110%的静息运动阈值(RMT)。该设置确保TMS能够有效地激活目标脑区,同时避免过度刺激可能带来的不适。为了提高TMS-EEG记录中的信噪比,实验中总共设置105个单脉冲。
2、EEG记录
实验中使用了64通道的德国Brain Products脑电放大器(瀚翔脑科学为BP脑电国内唯一代理商)记录连续的EEG信号。记录的采样率为5000Hz,它确保了能够捕捉到高时间分辨率的脑电活动。在记录过程中,以FCz和AFz作为参考和地电极。
3、数据分析
在数据分析之前,数据首先根据TMS脉冲进行分段(-1000ms到1000ms),并进行基线校正(-500ms到-10ms)。实验中使用显著电流密度(SCD)和显著电流传播(SCS)来分别分析局部电流和电流传播。
源活动是通过线性约束最小方差(LCMV)波束形成器计算得出的。LCMV波束形成器是一种先进的信号处理技术,能够有效地从EEG信号中提取特定脑区的源活动。这种技术的应用使得研究者能够更准确地定位TMS诱发的脑电活动的起源,从而为进一步的神经机制研究提供重要依据。
4、ROI
为了全面研究与疼痛相关的结构,实验中基于神经病理性疼痛矩阵选择了4个结构作为源空间中的ROI。这些结构包括感觉痛觉结构(如丘脑腹后核、初级体觉皮质、顶叶皮层、后岛叶和中扣带回皮层)、注意力认知结构(如丘脑内背侧核、背外侧前额叶、前岛叶和胼胝体上部前扣带回)、情感疼痛结构(如眶额叶、前扣带回、亚扣带回和腹侧纹状体)以及下行结构(如中脑导水管周围灰质)。
这些ROI的选择涵盖了与疼痛感知、注意力、情感以及下行调节相关的多个关键脑区,为研究神经病理性疼痛的神经机制提供了全面的视角。
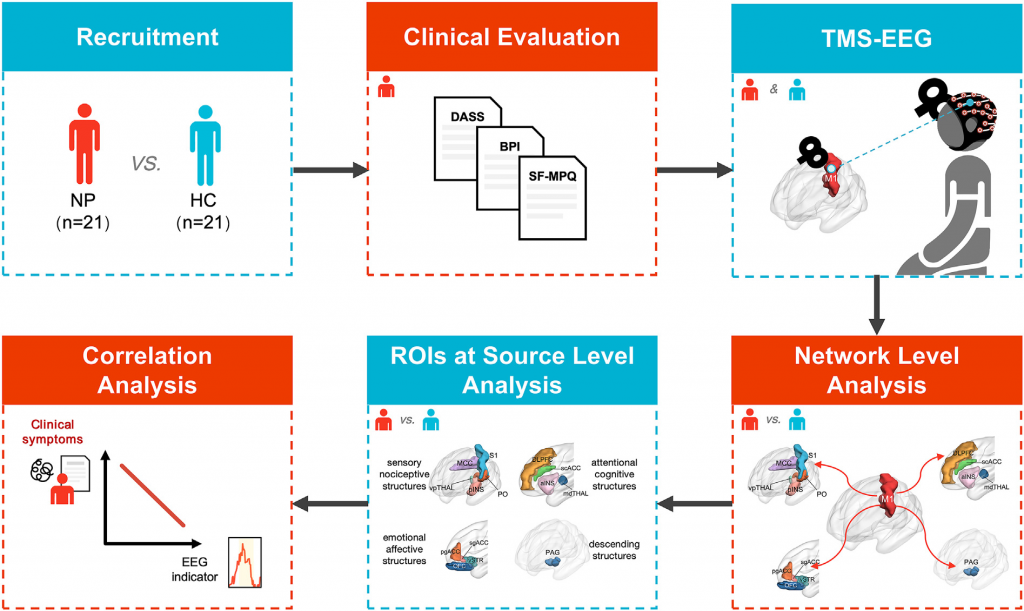
图1 研究流程图
三、研究结果
1、电流传播的异常模式
(1)感觉痛觉结构
与健康对照组相比,神经病理性疼痛患者在感觉痛觉结构中表现出显著的电流传播异常。M1至初级体觉皮质(S1)的电流传播显著增强,这一异常传播主要集中在220 - 240ms的时间窗内。表明在神经病理性疼痛状态下,运动皮层对感觉痛觉相关脑区的激活模式发生了改变,可能与疼痛感知的异常增强有关。
(2)注意力认知结构
在注意力认知结构方面,神经病理性疼痛患者同样呈现出独特的电流传播特征。M1至前岛叶(aINS)和胼胝体上部前扣带回(scACC)的电流传播显著增加,且这一现象同样集中在220 - 240ms的时间段。这提示神经病理性疼痛可能影响了大脑对疼痛相关注意力和认知资源的分配,导致患者对疼痛的注意力过度集中以及认知加工过程的异常。
(3)情感疼痛结构
情感疼痛结构中的电流传播异常同样引人注目。神经病理性疼痛患者在M1至眶额叶皮层(OFC)、前扣带回皮层(pgACC)和亚扣带回皮层(sgACC)的电流传播显著高于健康对照组,异常传播的时间段同样锁定在220 - 240ms。这一结果揭示了神经病理性疼痛与情感疼痛相关脑区之间的异常连接。
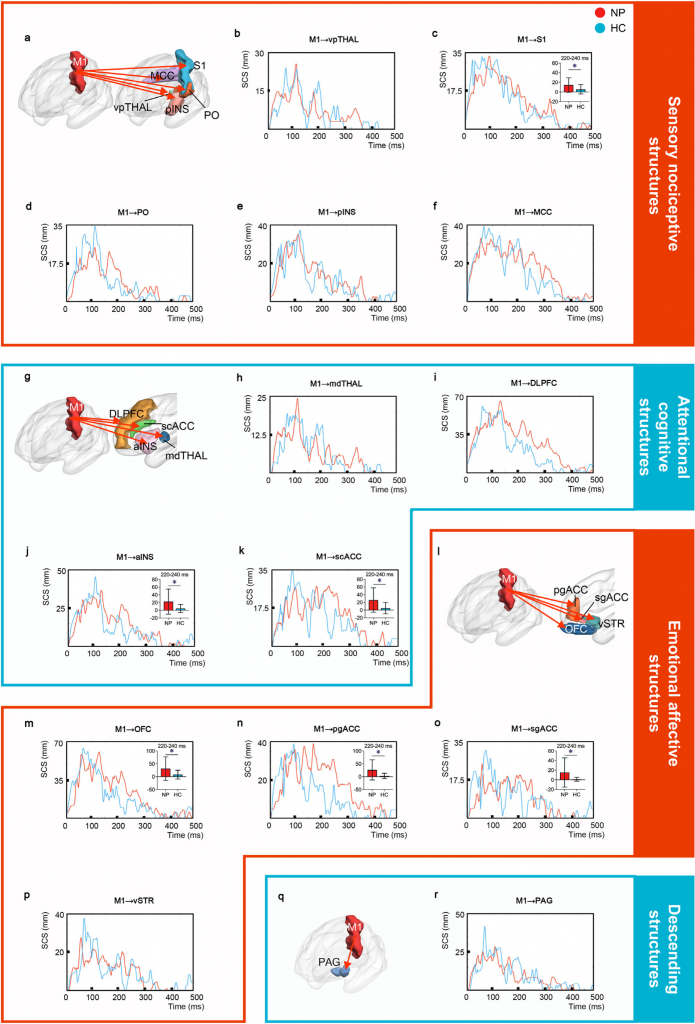
图2 显著电流传播:神经病理性疼痛vs健康人群
2、局部电流密度的改变
(1)感觉痛觉结构
在感觉痛觉结构中,神经病理性疼痛患者初级体觉皮质(S1)的局部电流密度显著低于健康对照组,异常出现在110 - 130ms的时间范围内。这可能意味着在神经病理性疼痛状态下,初级体觉皮质对TMS刺激的反应性降低,其在疼痛信号处理过程中的功能可能受到抑制,进而影响了疼痛感知的准确性。
(2)注意力认知结构
与感觉痛觉结构不同,神经病理性疼痛患者在注意力认知结构中的局部电流密度呈现出显著增高的趋势。背外侧前额叶皮层(DLPFC)、前岛叶(aINS)和胼胝体上部前扣带回皮层(scACC)的电流密度均显著高于健康对照组,且异常主要集中在220 - 240ms的时间段。这表明在神经病理性疼痛状态下,这些与注意力和认知功能相关的脑区对TMS刺激的反应性增强,可能反映了大脑在疼痛情境下对注意力和认知资源的过度动员,以应对疼痛带来的挑战。
(3)情感疼痛结构
在情感疼痛结构中,神经病理性疼痛患者前扣带回皮层(pgACC)的局部电流密度显著高于健康对照组,异常同样出现在220 - 240ms的时间窗口。这一结果进一步强调了情感疼痛相关脑区在神经病理性疼痛中的异常激活,可能与患者疼痛体验中的情感成分加剧有关,如焦虑、抑郁等负面情绪的加重。
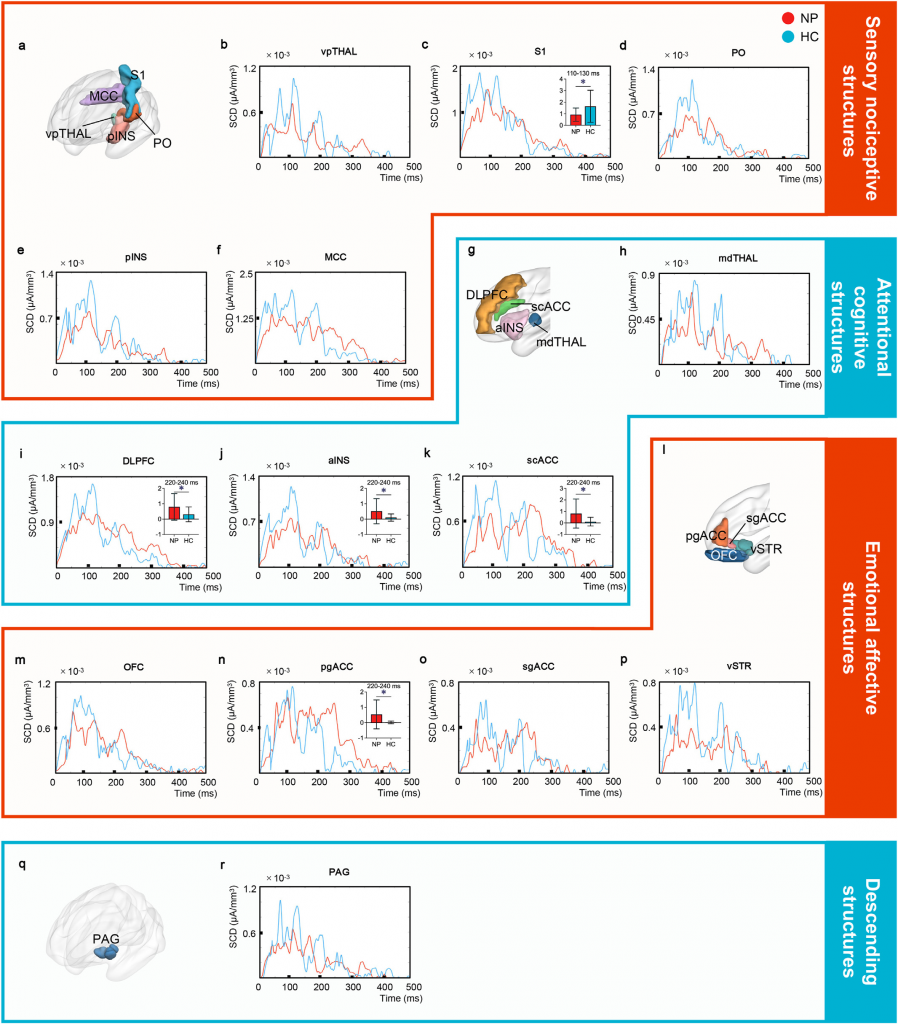
图3 显著电流密度:神经病理性疼痛vs健康人群
3、电流传播与疼痛体验的关联
通过皮尔逊相关性分析发现M1至前岛叶(aINS)的电流传播强度与情感疼痛体验量表之间存在显著的正相关关系。这意味着电流传播的增强与患者情感疼痛体验的加重密切相关,提示了前岛叶在神经病理性疼痛情感成分中的重要作用。
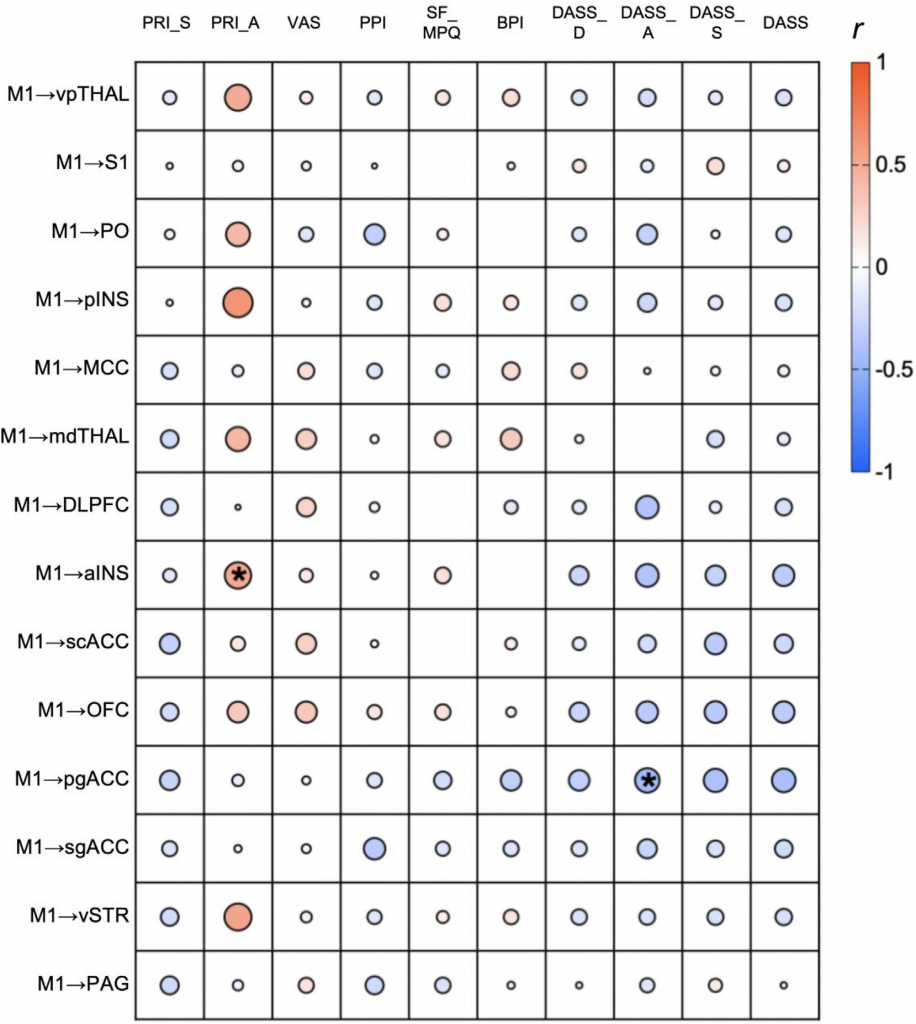
图4 显著电流传播与量表的相关结果
四、研究结论
研究表明运动皮层(M1)与前扣带回皮层(pgACC)之间的超连接性与较少的疼痛负面情绪相关,这意味着,通过调节这一特定神经回路的活动,可能有助于减轻神经病理性疼痛患者的情感负担,从而提升治疗效果。此外,研究还指出,rTMS对疼痛情感的影响可能通过调节多巴胺能传输实现,这为未来的治疗策略提供了新的靶点。
除了情感疼痛结构外,研究还揭示了神经病理性疼痛患者在感觉痛觉和注意力认知结构中的异常活动。因此,未来的治疗策略不仅应关注情感疼痛结构,还应考虑对感觉痛觉和注意力认知结构的综合调节,以实现更全面的治疗效果。